Sự điện li biểu thị quá trình phân ly các chất trong nước thành các ion âm và ion dương (hay được gọi là anion và cation). Các chất điện ly khiến cho các dung dịch như muối, axit, bazơ có thể dẫn điện. Nếu bạn đang quan tâm đến sự điện li và các chất điện li thì tìm hiểu chi tiết thông qua bài viết dưới đây của chúng tôi nhé.
1. Sự điện li là gì? Chất điện li là gì?
Đây là quá trình phân li của các chất trong nước hoặc khi các chất bị nóng chảy. Sản phẩm của các phân tử chất điện li tan trong nước sau khi trải qua quá trình điện li là các cation (ion dương) và anion (ion âm). Gọi chung những ion này là chất điện li, chúng được tách ra từ phân tử điện li, có khả năng dẫn điện dung dịch. Vì thế nhiều người gọi các dung dịch dẫn điện là chất điện li, tuy nhiên chúng chỉ là hợp chất hóa học, không phải nguyên tố.

Sự điện li là quá trình phân li của các chất trong nước hoặc các chất bị nóng chảy
2. Tính chất của chất điện li
Để hiểu thêm về sự điện li và chất điện ly, ta phải lấy axit, bazơ và muối ra làm ví dụ. Axit, bazơ và muối đều là các chất điện li (tan được trong nước). Khi ở trong dung dịch, các hợp chất hóa học này sẽ bị phân li (một phần hoặc toàn bộ). Sau đó trở thành các nguyên tử (hoặc nhóm nguyên tử) tích điện gọi là ion. Ion có khả năng chuyển động tự do trong dung dịch, trở thành hạt tải điện. Dưới đây là sự điện li của một số hợp chất mà bạn nên biết:
- Axit → gốc axit (ion âm) + H+.
- Bazo → OH– (ion âm) + ion dương (kim loại).
- Muối → gốc axit (ion âm) + ion dương (kim loại).
- Một số bazơ không chứa ion kim loại nhưng bị phân li thành ion trong dung dịch (Anion, cation,…).
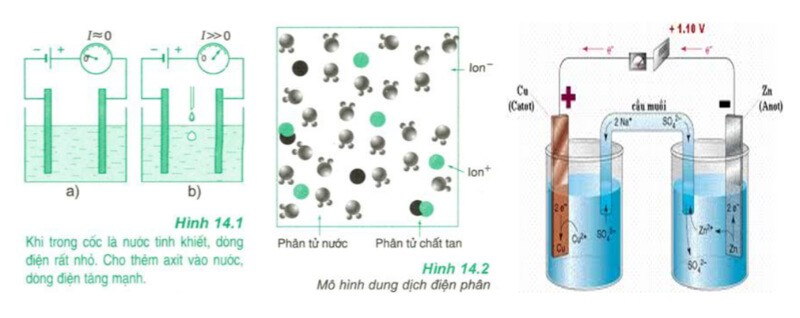
Tính chất của chất điện li là bị phân li (một phần hoặc toàn bộ) rồi trở thành ion
3. Phân loại các chất điện li phổ biến
Hiện nay chất điện li được phân thành 2 loại phổ biến nhất, đó là chất điện li mạnh và chất điện li yếu. Cụ thể:
3.1. Chất điện li mạnh
Những chất điện li mạnh sẽ tan hoàn toàn trong nước, các phân tử hoà tan sẽ phân li ra ion. Nhóm này sẽ bao gồm các hợp chất axit mạnh, bazơ tan, một số loại muối như:
- Các axit mạnh: HBr, HI, HCl, HNO3, H2SO4, HClO4, HClO3…
- Các bazơ tan: Ba(OH)2, NaOH, KOH, Ca(OH)2,…
- Một số loại muối: CuSO4, NaCl, KNO3…
Phương trình điện li của các chất điện li mạnh sẽ sử dụng mũi tên 1 chiều (→). Ví dụ như sau:
- H2SO4 → 2H+ + SO4 (2-).
- KOH → K+ + OH-.
- Na2SO4 → 2Na+ + SO4 (2-).

Chất điện li mạnh
3.2. Chất điện li yếu
Những chất điện li yếu cũng tan trong nước nhưng chỉ có một số phân tử hoà tan sẽ phân li thành ion, những phân tử còn lại vẫn tồn tại trong dung dịch. Nhóm chất điện li yếu sẽ bao gồm các axit trung bình, bazơ không tan như:
- Các axit trung bình và yếu: HCOOH, H2S, H2CO3, H3PO4,…
- Các bazơ không tan: Fe(OH)2, Fe(OH)3, Mg(OH)2,…
Phương trình điện li của chất điện li yếu sẽ sử dụng 2 mũi tên ngược chiều (⇌). Sự điện li của nhóm chất điện li yếu được đánh giá bằng đại lượng độ điện li α. Ví dụ như sau:
- H2S ⇌ H+ + HS-.
- α = Số phân tử phân li hoặc tổng số phân tử đã hoà tan.

Chất điện li yếu
4. Tổng hợp một số bài tập hóa học phổ biến về sự điện li
Để bạn hiểu rõ hơn về sự điện li, dưới đây chúng tôi đã tổng hợp lại một số bài tập đã bao gồm cách giải. Bạn hãy tham khảo để có cái nhìn tổng quát hơn về sự điện li và chất điện ly nhé. Cụ thể:
Bài tập 1
Trong “Sách giáo khoa Hóa học lớp 11” tại trang 7, bài 1 ghi “Các dung dịch bazơ như NaOH, axit như HCl, muối như NaCl dẫn điện được. Vậy các dung dịch như saccarozơ, glixerol, ancol etylic không dẫn điện được thì nguyên nhân chính là gì?”
Hướng dẫn giải
Trong dung dịch: Các bazơ, các muối, các axit sẽ phân li ra ion dương và ion âm chuyển động tự do, vì vậy dung dịch của chúng có khả năng dẫn điện. Ví dụ:
- HCl → H+ + Cl-.
- NaOH → Na+ + OH-.
- NaCl → Na+ + Cl-.
Còn những dung dịch như đường saccarozơ, glixerol, ancol etylic không dẫn điện bởi vì trong dung dịch chúng không phân li ra được các ion dương và ion âm.
Bài tập 2
Trong “Sách giáo khoa Hóa học lớp 11” tại trang 7, bài 3 ghi “Viết phương trình điện li của nhóm chất điện li mạnh. Bao gồm: Ba(NO3)2 0,10M; HNO3 0,020M; KOH 0,010M.”
Hướng dẫn giải
- Ba(NO3)2 → Ba 2+ + 2 NO3 −
0,10 0,10 0,20 ( M )
→ [Ba2+] = 0,1M; [NO3 −] = 0,2M
- HNO3 → H + + NO3 −
0,020 0,020 0,020 M
→ [H+] = [ NO3 − ] = 0,02M
- KOH → K + + OH −
0,010 0,010 0,010 M
→ [K+] = [OH-] = 0,010M
Bài tập 3
Trong “Sách giáo khoa Hóa học lớp 11” tại trang 7, bài 5 ghi “Chất nào dưới đây không dẫn điện được? Khoanh tròn vào đáp án đúng:
- CaCl2 nóng chảy.
- HBr hoà tan trong nước.
- NaOH nóng chảy.
- KCl rắn, khan.”
Hướng dẫn giải:
Câu trả lời chính xác bạn cần khoanh tròn đó là đáp án D. Do KCl rắn, khan. Bởi vì chúng tồn tại dưới dạng mạng tinh thể ion, rất bền vững. Những chất này sẽ không phân li ra được ion dương và ion âm (di chuyển tự do) khi ở trong dung dịch, do đó chúng không có khả năng dẫn điện.
Mong rằng sau khi đọc bài viết này, bạn đã hiểu rõ về sự điện li và chất điện ly. Chúc bạn áp dụng những thông tin được chia sẻ ở bài viết này để hoàn thành thật tốt chương trình hóa học và vật lý phổ thông của mình nhé!



