Nồng độ mol là gì,cóbao nhiêudạng bài tậpphổ biến,haygặp trongmônhoá học trung học. Vậy nó được tínhthế nào? Hãy cùng Acuonggroup tìm hiểucụ thểtrong bài viếtdướiđâytham khảomột vàibài tậpứng dụngđểnắmvữngthêmnha.
Nồng độ mol là gì?
Nồng độ mol biểu thị cho số mol của một chấthoà tantrong một lítthuỷdịch, nó đượcký hiệulà M
Ví dụ: Trong 4 lít dung dịch chứa 2 mol hạt tan tạothànhdung dịch 0,5 M hay còn gọi là 0,5 phân tử gam.
Ngày nay mol đượcsử dụngphổ biếntrong hoá họcnhằmbiểu thịsố lượngchấtphản ứng hoá họcvàkết quảcủa cácquá trìnhhoá học. Ngoài ra, nócũngđượcdùngđểchỉtổng sốelectron, các thực thể kháccótrong một mẫu nhất định của một chất hay ion.

Nồng độ mol là gì
>>>XEM THÊM: Chất thải nguy hại – Phân loại, mã màu quy định và cách xử lý
Chất thải nguy hại – Phân loại, mã màu quy định và cách xử lý
Công thức tính nồng độ mol
- Ta có công thức:
CM = n/ Vdd
Trong đó:
- CM là nồng độ mol
- n là số mol chất tan
- Vdd là thể tích dung dịch (đơn vị tính: lít)
Công thức tính số mol đơn giản
1. Cách tính số mol qua thể tích
n = V/22.4
Trong đó:
- n là số mol chất khí tại điều kiện tiêu chuẩn (đktc) với đơn vị tính: mol
- V: thể tích của chất khí ở đktc (tính bằng lít)
2. Tính số mol thông qua khối lượng
n = m/M
Trong đó:
- n là số mol, có đơn vị tính là mol
- m là khối lượng được tính bằng gam
- M là khối lượng mol chất, tính bằng g/mol
3. Một số cách tính khác
| Điều kiện | Công thức | Chú thích | Đơn vị tính |
| Khi có nồng độ mol/lít | n = CM.V | – n: số mol chất | mol |
| – CM: nồng độ mol | Mol/lit | ||
| – V: thể tích dung dịch | lit | ||
| Khi biết số nguyên tử hay phân tử | n = A/N | – A: số nguyên tử hay phân tử | Nguyên tử hoặc phân tử |
| – Số Avogadro (số đơn vị trong bất cứ một mol chất nào và có giá trị bằng 6.1023) | |||
| Tính số mol khí tại điều kiện thường | n = P.V/R.T | – P: Áp suất | 1 atm = 760mmHg |
| – V: thể tích khí | Lít | ||
| – R: hằng số | 0,082 (hoặc 62400) | ||
| – T: nhiệt độ tính theo độ Kelvin (K) | K = 273 + độ C |

Có rất nhiều cách tính số mol
Tham khảo một số bài tập tính nồng độ mol
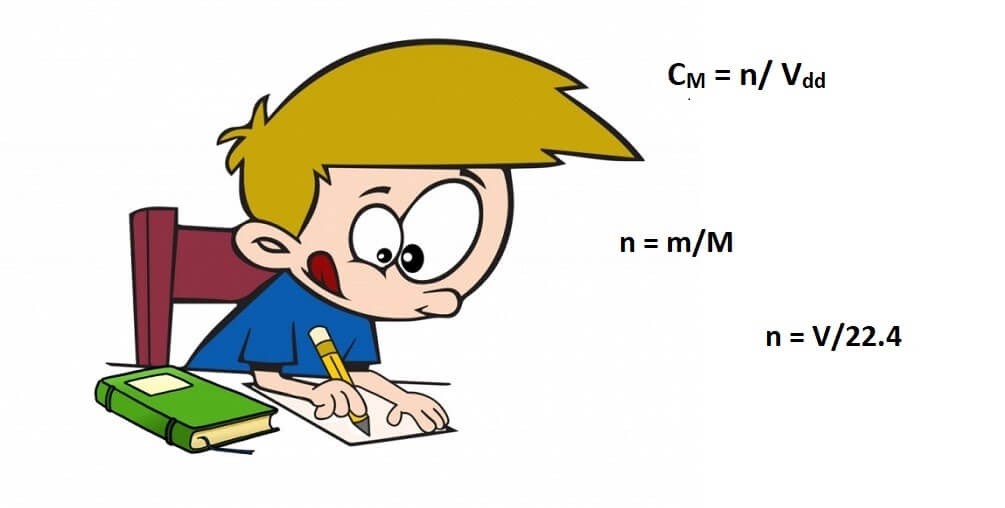
Một số bài tập tham khảo về cách tính nồng độ mol:
Bài tập 1: Trong 400ml dung dịch có hòa tan 32 gam chất NaOH. Hãy tính nồng độ mol của dung dịch
Lời giải:
- Đổi 400 ml = 0,4 lít
- nNaOH = 36/40 = 0,9 mol
- Theo công thức tính CM ta có:
- Cdd = n/V = 0,9/0,4 = 2,25 (M)
Bài tập 2: Tính CM của 0,5 mol MgCl2 có trong 1,5 lít dung dịch
Lời giải:
- Áp dụng vào công thức tính CM ta có:
CM = 0,51 x 5 = 0,33 (mol)
Bài tập 3: Tính nồng độ mol của một dung dịch chứa 0,5 mol NaCl trong 5 lít dung dịch.
Lời giải:
CM = 0,5/5 = 0,1 (mol)
Bài tập 4: Hãy tính nồng độ mol của dung dịch khi tiến hành hòa tan 15,8g KMnO4 trong 7,2 lít nước.
Lời giải:
- Số mol của chất nKMnO4 là:
nKMnO4 = 15,8/ 158 = 0,1 (mol)
- Vậy CM sẽ bằng: 0,1/ 7,2 = 0,0139
Bài tập 5: Tiến hành cho 6,5 gam kẽm phản ứng vừa đủ với 100 ml dung dịch axit chohidric (HCl). Hãy:
- a) Tính thể tích của H2 thu được ở điều kiện tiêu chuẩn
- b) Tính nồng độ mol của dung dịch HCl đã sử dụng
Lời giải:
- Theo bài ra ta có:
nZn = 6,5/ 65 = 0,1 mol
- Phương trình phản ứng:
Zn + 2HCl → ZnCl2 + H2
- nZn = nZnCl2 = 0,1 mol
- nHCl = 2nZn = 0,2 mol
- a) VH2 = 0,1 x 22,4 = 2,24 (lít)
- b) CddHCl = 0,2/ 0,1 = 2 (M)
Trên đây, Acuonggroup đã giới thiệu cho bạn đọc chi tiết về nồng độ mol là gì cũng như cách tính và một số bài tập vận dụng cơ bản. Mong rằng, qua bài viết đã giúp bạn hiểu rõ hơn các vấn đề này và có thể áp dụng trong học tập hay công việc. Truy cập webthường xuyên để đón đọc nhiều bài viết hữu ích khác.



